-
목차
본 논문은 본 블로그 운영자인 필자가 2024년에 작성하고 논문 투고 시기를 놓쳐 게재하지 않은 논문의 final 버전입니다. AHP 방법론과 분산형 임상시험에 관심있는 분이라면 참고하셔도 좋습니다!
AHP 방법론을 활용한 분산형 임상시험 법제 개선 연구
Using The Analytic Hierarchy Process (AHP) Methodology To Research Legislative Improvements For Decentralized Clinical Trials
Purpose: As of 2022, global pharmaceutical companies are actively adopting 'Decentralized Clinical Trials (DCTs)' that eliminate physical distance restrictions. A clinical trial conducted remotely for a significant portion or the entire process—from patient recruitment to specimen acquisition to monitoring—is known as DCT. This approach is gaining popularity rapidly due to its advantages, such as recruiting diverse participants, reducing costs, enhancing patient convenience, and enabling centralized management in multinational trials. However, in Korea, decentralized clinical trials are currently deemed illegal, as clinical trials are permitted only within designated institutions under the Pharmaceutical Affairs Act. In contrast, many countries, including the United States, Europe, and China, are attracting the demand for clinical trials from global pharmaceutical companies through swift regulatory actions. Korea is also working on system reviews and pilot projects to permit decentralized clinical trials. Nevertheless, this process requires more time as it necessitates overhauling related laws, such as the Pharmaceutical Affairs Act. This study aims to formulate a plan for regulatory improvements by amending the Pharmaceutical Affairs Act.
Method Through a literature review and the collection of expert opinions using the Analytic Hierarchy Process (AHP), the study identifies the importance and priority of these improvements to expedite the government's introduction of a decentralized clinical trial system.
Result The conclusion is clear: the DCT introduction policy should be implemented, with the foremost priority being the amendment of the legal system to allow clinical trials outside designated clinical trial institutions.
Key words: Decentralized Clinical Trial, Pharmaceutical Affairs Act, Medical Act, Regulatory Reform, AHPSummary
The world is rapidly adopting the Decentralized Clinical Trials (DCTs) approach in clinical trials to advance drug development. If we ignore these global trends and continue to rely solely on traditional methods, Korea's position as a leader in global clinical trials could quickly deteriorate. To expedite the legal reforms necessary for enabling DCT, this study identified the highest-priority system improvements for DCT introduction through a review of existing research. Additionally, an expert survey using the Analytic Hierarchy Process (AHP) technique was conducted to assess the priority and importance of these tasks. The study ultimately determined that the DCT introduction policy should be implemented. The top priority for achieving this is to amend the legal system to allow clinical trials outside of established clinical trial institutions.
Ⅰ. 서론
1. 연구배경 및 목적‘분산형 임상시험(Decentralized Clinical Trial, DCT)’은 임상시험 관련 활동의 일부 또는 전부가 기존 임상시험 기관이 아닌 다른 위치에서 발생하는 임상시험을 의미한다(null, 2024). 신약개발 기술에 정보통신기술을 접목해 임상시험대상자 모집부터 검체 획득, 모니터링 등 임상시험 과정의 전부 또는 일부를 원격으로 진행하는 임상시험이다. 특히, 원거리 참가자 모집과 이에 따른 비용 절감, 환자의 편의성 증대, 중앙 집중형 관리 등의 여러 장점이 있다. DCT는 이러한 장점으로 코로나19 팬데믹 기간 중 코로나19를 예방하는 백신 개발 임상시험 방법으로 사용되거나, 중단되었던 의약품 개발을 지속하는데 중요한 역할을 담당했다.
서울은 최근 6년 연속해서 전 세계 도시 중 가장 많은 임상시험을 수행한 도시로 기록됐으며, 단일 국가 임상시험 순위로는 2023년 미국, 중국, 다음으로 3위를 기록할 만큼 우리나라는 임상시험 선도국이라고 할 수 있다(https://www.mfds.go.kr). 또한 ITU (International Telecommunication Union)의 발표에 따르면, 2022년 기준 우리나라는 인터넷공급망(Network coverage) 100%, 휴대폰 보급률(Mobile phone ownership) 97%, 가정내 ICT 접근(ICT access at home) 100% 등 디지털 연결성이 세계 최고를 기록할 만큼 정보통신기술 강국이다(https://www.itu.int/). 따라서 임상시험 기술에 정보통신기술을 접목한 DCT를 아직 도입하지 못한 것은 매우 의아한 일이다.
이런 가운데, 각국의 규제기관들은 앞다투어 공공-민간 협력을 통해 규제를 마련하고 복잡한 임상시험 환경을 헤쳐나가기 위해 노력하고 있다. 미국 식품의약품안전국(Food and Drug Administration, FDA)과 듀크대학교는 2007년에 설립한 Clinical Trials Transformation Initiative (CTTI)를 통해 민간 기업 80개사와 함께 DCT와 같은 새로운 임상시험 주제들에 대한 권고안 및 도구를 개발했으며(https://ctti-clinicaltrials.org), 유럽연합은 2022년, EC-HMA-EMA의 협의체로 ACT EU (Accelerating Clinical Trials in the EU)를 설립하고, 10개의 중요실천과제에 DCT를 포함하여 규제를 개선하고 있다(https://www.ema.europa.eu).
따라서, 우리나라가 임상시험 선도국을 유지하고 이를 바탕으로 제약산업의 성장과 발전을 견인하기 위해서는 의약품 개발과 관련된 이른바, 급속도로 발전하는 기술혁신의 속도를 법・제도의 변화속도가 따라가지 못하면서 발생하는 현상인 ‘규제지체 현상(이종한 등, 2020)’을 신속하게 해소해야 한다. 본 연구는 이를 위해 무엇보다 DCT와 관련된 제도를 파악하고 DCT 도입을 가로막고 있는 규제는 무엇인지, 또한 해당 제도를 개선하는 데 있어 우선순위를 도출하는 것을 목적으로 하고 있다.2. 선행연구
윤계형(2020)은 『의약품 임상시험 안전 관련 법제 개선연구』를 통해 의약품 임상시험의 안전성을 효율적으로 확보하기 위한 법제의 개선 방향으로 「약사법」을 수정·보완하는 것만으로는 시대적 상황변화를 대처하기 어렵다고 보고, 가칭 「의약품 임상시험에 관한 법률」을 제정할 것을 주장했다. 하지만, 보고서가 출판되었던 2020년은 DCT가 전통적 임상시험의 대안으로 채택되어 폭발적으로 증가하던 시기였던 만큼 보고서에 DCT에 대한 언급이 없었던 것은 아쉬운 부분이다. 이은영(2020)도 『임상시험 관련 법제의 문제점과 개선방안』에서 일본의 「임상연구법」과 같이 의약품뿐 아니라 의료기기에 관한 임상연구를 포함하는 통합 제정법을 제안하면서, 이를 통해 규정이 없거나 지침에 머물렀던 내용을 법률로 승격시켜야 한다는 주장을 함으로써, DCT의 출현과 규제지체 해소의 필요성은 인식하지 못한 채 「약사법」 중심의 임상시험 제도의 불합리성을 상기하는 정도에 그쳤다.
우리나라에서 발표된 연구 중 DCT에 대한 정확한 이해와 제도적 도입을 주장한 연구는 김영호(2022년)가 유일하다. 김영호(2022)는 『분산형 임상시험(Decentralized Clinical Trial): 장점과 사례 중심으로』에서 DCT의 개념과 장점을 소개하며, 실제 DCT 개념을 활용한 임상시험 사례를 제시하고, 완전한 DCT가 어렵다면 임상2상부터 적용할 것을 제안하였다.
DCT 제도의 도입에 대한 연구가 아닌 DCT 방법으로 직접 연구자 임상을 수행한 사례가 있다. 허기영(2023)은 『Factors influencing the reliability of decentralized elements in clinical trials: results of three prospective studies = 임상시험에서 분산형 요소의 신뢰성에 영향을 미치는 요인: 세 가지 전향적 연구 3건의 결과에 기반하여』를 통해 비타민 D가 결핍된 성인을 대상으로 12주 동안 DCT를 실시한 바 있다. 허기영은 임상시험용의약품으로 건강기능식품인 유산균과 비타민 C 보충제를 사용함으로써 현행 「약사법」상 의약품 배송이 불가능하다는 일각의 법 해석을 우회적으로 극복했다.3. 이론적 배경
코로나19 팬데믹을 기점으로 임상시험은 새로운 전환기를 맞았다. 이전 시기의 임상시험은 대상자가 임상시험실시기관에 방문하여 임상시험에 대한 설명, 서면 동의서 작성, 임상시험용의약품 수령 후 투약 등으로 임상시험이 수행되었지만, 코로나19 팬데믹 시기 임상시험대상자의 이동이 제한되면서 임상연구가 중단되거나 연기되는 사례가 급격하게 늘어났다. 새롭게 임상시험을 시작하려 해도 대상자 모집이 어려워 연구를 아예 포기하는 기업들이 생겨났다. 세계 각국은 이를 극복하기 위해 재빨리 DCT를 채택하기 시작했다. Izem R.(2024), Chodankar D 등(2024)은 DCT에 대한 업계와 규제 당국의 관심은 그보다 오래되었지만, 코로나19 팬데믹으로 인해 이러한 DCT의 채택과 경험이 가속화되었다고 보고 있다.
미국 FDA는 임상시험 관련 활동의 일부 또는 전부가 전통적인 임상시험 실시기관 이외에서 일어나는 것을 DCT로 정의하고 있다(https://www.fda.go). 모든 절차를 꼭 원격으로 할 필요는 없다는 것이다. DCT의 다양한 요소 중 하나 이상을 활용하면 DCT라고 할 수 있다. 또한, 임상시험 실시기관 외에서 수행되는 것으로 정의하는 만큼 반드시 ‘디지털’, ‘비대면’, ‘원격’이 수행되어야 한다는 의미는 아니다. DCT는 항상 디지털이나 원격은 아니지만 적어도 일부 요소가 그러하다는 것이며, 전체적으로 환자가 좀 더 편하게 임상시험을 할 수 있도록 하는 것이다.
우리나라 정부도 2023년 12월 세계적인 추세인 DCT를 도입하기 위해 「임상시험 전자동의 가이드라인」을 개정했지만(https://www.mfds.go.kr) 이는 DCT의 완전한 제도적 도입과는 여전히 거리가 있다. DCT 방식 중에서 전자동의는 가장 기초적인 요소라고 할 수 있으며, 이 밖에도 해결해야 하는 개선사항들이 산적해 있기 때문이다.
전자동의와 같은 기초적인 사항 외에도 제도적으로 DCT를 도입하기 위해 제안된 개선과제들에는 어떤 것들이 있는지 알아보기 위해 공공 또는 민간 기관에 의해 수행된 DCT 관련 연구보고서와 발표자료를 수집·분석하였다. 검토 결과, DCT를 도입하기 위한 개선과제들은 4개 영역의 과제들로 분류되었다. 개선과제 분류는 연구자들이 제시한 정책제언, 개선방안 등을 참조하여 정리하였다. 문헌검토를 통해 추출한 4개 영역은 1) 임상시험실시기관 외 임상시험 허용, 2) 임상시험용의약품의 원격처방 허용, 3) 임상시험용의약품의 택배 배송 허용, 4) 방문간호사 검체채취 허용이다.
표 1. DCT 도입을 위한 개선과제번호 개선과제 비고 1 임상시험실시기관 외 임상시험 허용 약사법 개정 필요 2 임상시험용의약품의 원격처방 허용 복지부 지침 마련 필요 3 임상시험용의약품의 택배 배송 허용 약사법 개정 필요 4 방문간호사의 검체채취 허용 의료법, 의료법 시행규칙 개정 필요
아울러, 영역별 개선과제를 해결하기 위해서는 법령 개정 등이 필요할 것으로 판단했다. 예컨대, 임상시험실시기관 외 임상시험 허용은 「약사법」 제34조 제3항 제1호를 개정해야 하며, 임상시험용의약품의 원격처방 허용은 보건복지부가 별도의 지침을 마련해야 하며, 임상시험용이약품의 택배배송 허용은 「약사법」제50조 제1항을 개정해야 하고, 방문간호사의 검체채취를 허용하기 위해서는 「의료법」제2조 제2항 제5호 마목을 신설, 「의료법 시행규칙」제24조의2를 신설하는 개정을 해야 한다는 사실을 밝혀냈다.
Ⅱ. 연구방법
1. 분석방법본 연구는 임상시험과 관련된 집단을 대상으로 계층분석 방법인 AHP 방법을 활용하여 설문결과를 수집하고 분석하였다. 이 방법은 의사결정의 계층구조를 구성하고 있는 요소 간의 쌍대비교(pairwise comparison)를 통하여 평가자의 지식, 경험 및 직관을 포착하고자 하는 의사결정 방법론이다. AHP는 복잡한 다기준 의사결정 상황에서 수치화가 가능한 정량적 요소만이 아니라, 계량화가 어려운 정성적 요소를 동시에 의사결정에 반영할 수 있도록 해준다. AHP는 한 번에 비교해야 할 지표의 수가 많고, 평가지표 체계에 포함되어있는 지표들이 다수이며 복합적이어서 의사결정에 있어서 체계적인 비교를 하기가 쉽지 않을 때 사용한다. 이런 경우, AHP는 의사결정 문제를 단순화하고 체계화시킴으로써 합리적인 의사결정 도구의 역할을 한다. 또한, 각 계층에 있어서 각 기준 또는 하위기준 간의 상대적 중요도를 측정하는 것이 필요한데, 이 방법은 이원 비교행렬(pairwise comparison matrix)을 통해 일관성 있게 유도될 수 있다.
이 방법으로 어떠한 정책 대안이나 제도의 우선순위를 도출할 수 있고, 정책을 시행할지 말지를 결정할 수 있다. 또는, 어떠한 기능이나 역할, 직무에 대하여 우선순위를 도출할 수 있는데, 이 연구는 전자의 유형에 속한다고 볼 수 있다. 이러한 방법을 활용한 사례는 예비타당성조사가 있다. 박득(2015)은 한국개발연구원이 공공사업의 타당성 평가에서 AHP 기법은 기존의 공공사업의 평가가 비용편익분석에 의한 경제성 분석을 위주로 하였던 것에 비하여, 경제성 이외의 여러 가지 다른 정책효과들을 평가에 반영할 수 있으며, 다양한 정책적 효과에 대한 평가가 정성적인 평가로 제한되는 것이 아니라 정량적인 지표로 제시되고, 또 궁극적으로 정책적 효과와 경제성의 각각의 중요도에 대한 가중치 산정과정을 통해서 종합평가를 내리도록 함으로써 평가의 객관적인 기준이 명시적으로 제시된다는 점에서 공공사업의 타당성을 사전에 검토하는 예비타당성조사에서는 AHP 기법의 활용을 기본 방법론으로 제시하고 있다고 밝히고 있다.
AHP에 의한 상대적 중요도 측정을 위한 척도는 9점 척도를 이용한다. 이 척도를 이용하여 계층 각 단계의 요소를 비교하면서 이원비교 행렬표를 만들게 되는데, 이때 단계별 요소가 n개인 경우 n×(n-1)/2가지 이원비교를 하게 된다. 본 연구 계층 1에서는 요소를 4가지로 정하였으므로, 4×(4-1)/2 즉, 6가지 이원비교를 하였으며, 계층 2에서는 4가지 기준에 대한 정책 시행과 미시행을 1회씩 비교했다. 수집된 설문지는 코딩작업을 거쳐 통계 처리하였는데, 일관성 분석과 상대적 중요도는 온라인으로 제공되는 ‘AHP Online System –AHP-OS’ 프로그램을 활용하여 분석하였다. AHP 조사는 1회 실시하였으며, 조사는 전자 메일을 통하여 2024년 5월 30일부터 6월 5일까지 실시하였으며, 패널들은 조사 문항에 대해 한 문항도 빠짐없이 전부 응답하였다.2. 조사대상
본 연구에서 조사대상은 대부분 임상시험 산업 분야의 경력 10년 이상의 임상 연구자와 제약업계 전문가로 구성했다. 가령, 임상약리학 등을 전공한 의사 3명, 임상시험 정책을 연구하는 기관·단체(식품의약품안전처, 국가임상시험지원재단, 한국CRO협회, 한국바이오의약품협회) 전문가 5명, 국내외 제약업계 및 제약유통업계(한미약품, LG화학, 쥴릭파마) 3명 총 11명이었다. 전문가들의 경력은 평균 22년으로 임상시험 산업에 대한 이해도가 매우 높은 전문가들이다(<표 2> 참조).
표 2. 조사대상구분 성별 분야 경력 (year) 남 여 학계 기관·단체 업계 1〜3 3〜5 5〜10 10 이상 명 6 5 3 5 3 0 1 2 8 비율(%) 54.6 45.4 27.2 45.4 27.3 0 9.1 18.2 72.7 3. 계층구성
DCT 제도적 도입에 대한 계층 1의 요소는 총 4가지로, 요소 1은 ‘임상시험실시기관 외 임상시험 허용’, 요소 2는 ‘임상시험용의약품의 원격처방 허용’, 요소 3은 ‘임상시험용의약품의 택배 배송 허용’, 마지막으로 요소 4는 ‘방문간호사의 검체채취 허용’으로 하였다. 계층 2에서 대안 1은 ‘정책 시행’, 대안 2는 ‘정책 미시행’으로 예비타당성조사에서처럼 정책을 시행할 것인지, 시행하지 않을 것인지로 구분했다.
그림 1. 계층구성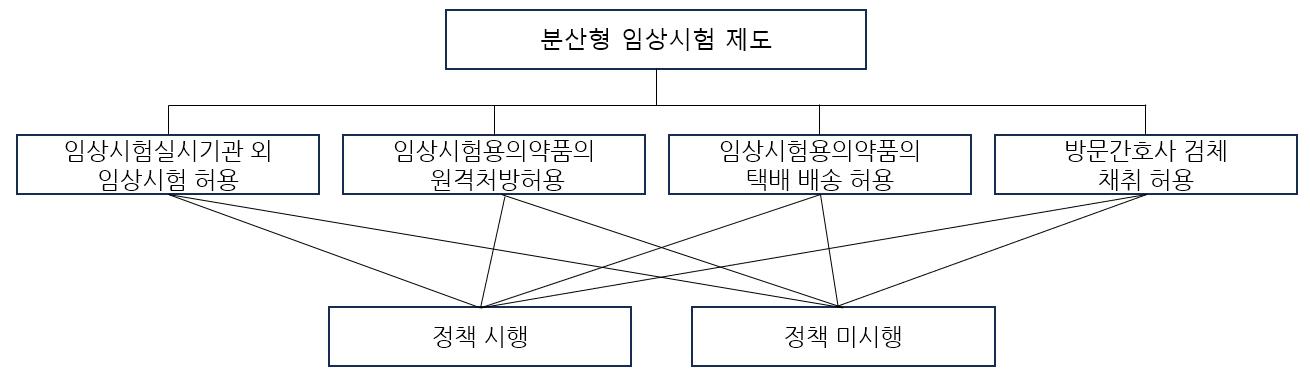
계층구성 4. 법령개정안 예시
평가자들의 이해를 돕기 위해 계층 1의 요소들의 의미를 설명하는 법령개정안 예시를 <표 3>과 같이 AHP 설문조사지 기재하였다.
표 3. 각 기준 별 법령개정안 예시
계층 1 요소 법령개정안 예시 요소 1 임상시험실시기관 외 임상시험 허용 「약사법」 제34조 제3항 제1호 개정;
제34조의2제1항에 따라 지정된 임상시험실시기관 또는 임상시험검체분석기관에서 임상시험을 실시할 것. 다만, 임상시험의 특성상 원격으로 데이터 수집이 가능하여 임상시험대상자의 현 거주지 또는 임상시험대상자의 편의를 고려한 장소에서 실시한다는 계획을 식품의약품안전처장이 승인한 임상시험이거나, 임상시험실시기관 또는 임상시험검체분석기관이 아닌 의료기관의 참여가 필요하다고 인정되는 총리령으로 정하는 임상시험은 그러하지 아니하다.요소 2 임상시험용의약품의 원격처방 허용 보건복지부 지침 마련;
보건복지부 공고 제2020-177호「전화상담·처방 한시적 허용방안」과 유사한 형태로, 식품의약품안전처장이 계획을 승인하여 안전성 확보가 가능한 분산형 임상시험의 경우, 임상시험대상자가 의료기관을 직접 방문하지 않고도 임상시험용의약품을 원격으로 처방받을 수 있도록 하는 보건복지부 지침 마련요소 3 임상시험용의약품의 택배 배송 허용 「약사법」제50조 제1항 개정;
약사법 제50조 제1항: 약국개설자 및 의약품판매업자는 그 약국 또는 점포 이외의 장소에서 의약품을 판매하여서는 아니 된다. 다만, 시장ㆍ군수ㆍ구청장의 승인을 받은 경우와 임상시험의 특성상 원격으로 데이터 수집이 가능하여 식품의약품안전처장이 승인한 임상시험의 임상시험용의약품의 배송은 예외로 한다.요소 4 방문간호사의
검체채취 허용「의료법」제2조 제2항 제5호 마목 신설;
의료법 제2조제2항제5호마목 신설: 마. 임상시험실시기관에서 또는 임상시험대상자의 자택 등에서 임상시험계획서에 명시된 절차에 따라 임상시험 수행
「의료법 시행규칙」제24조의2 신설;
의료법 시행규칙 제24조의2 신설: 제24조의2(임상시험 방문간호) ① 법 제2조제2항제5호에 따라 간호사는 임상시험대상자의 자택 등을 방문하여 임상시험에 필요한 다음 각 호의 업무를 수행할 수 있다.
1. 검체의 채취 및 운반
2. 투약
3. 주사
② 임상시험 방문간호를 실시하는 간호사는 「전문간호사 자격인정 등에 관한 규칙」에 따른 임상전문간호사이어야 한다.
③ 임상시험 방문간호는 의사나 치과의사가 임상시험실시기관이나 검체분석기관 외의 장소에서 임상시험 수행이 필요하다고 판단하여 임상전문간호사에게 임상시험 수행을 의뢰한 자에 대하여만 실시하여야 한다.
④ 임상전문간호사는 임상시험 방문간호 중 검체의 채취 및 운반, 투약, 주사를 하는 경우에는 임상시험계획서에 명시된 절차를 따라야 한다.
⑤ 이 규칙에서 정한 것 외에 임상시험 방문간호의 질 관리 등 방문간호의 실시에 필요한 사항은 보건복지부장관이 따로 정한다.
위 개정안의 예시는 계층 1의 요소를 이해하는데 도움을 주는 수준의 참고용으로 작성하였으며, 법령 간 정합성 등은 심도 있게 고려하지 않았다. 그러나, 설문조사 결과 개정안에 대해 문제점을 제기하거나 별도의 수정(또는 반대)의견을 준 평가자는 없었다.
위 개정안에 대한 개략적인 설명은 다음과 같다. 첫째, 임상시험실시기관 외 임상시험 허용을 위해 「약사법」 제34조 제3항 제1호 개정안을 제시한 것은, 「약사법」 제34조가 임상시험의 계획 승인 등을 규정하고 있으며, 제3항이 임상시험을 하려는 자가 준수해야 할 사항들을 열거하고 있고, 제1호 규정이 임상시험실시기관과 검체분석기관에서만 임상시험을 하도록 했기 때문이다. DCT는 임상시험실시기관이 아닌 곳, 즉 임상시험대상자의 집이나 대상자의 편의를 고려한 장소에서 임상시험을 수행할 수 있도록 하는 것이므로, 임상시험실시기관 외 임상시험을 허용하기 위해서는 제1호 규정을 개정해야 한다. 따라서 제1호 규정의 예외 규정인 ‘임상시험실시기관 또는 임상시험검체분석기관이 아닌 의료기관의 참여가 필요하다고 인정되는 총리령으로 정하는 임상시험’과 함께, DCT 즉, ‘임상시험의 특성상 원격으로 데이터 수집이 가능하여 임상시험대상자의 현 거주지 또는 임상시험대상자의 편의를 고려한 장소에서 실시한다는 계획을 식품의약품안전처장이 승인한 임상시험’도 예외로 하는 안을 제시했다.
둘째, 임상시험용의약품의 원격처방 허용을 위한 보건복지부 지침을 마련할 것을 제안한 것은, 앞서 코로나19 팬데믹 기간 중 보건복지부가 공고 제2020-177호「전화상담·처방 한시적 허용방안」을 마련하여 의약품의 원격처방을 한시적으로 가능하게 한 것을 본 따 제안한 것이다. 보건복지부 지침 마련으로도 임상시험용의약품의 원격처방이 가능할 것이라고 보았기 때문이다. 물론, 「의료법」 제34조 먼 곳에 있는 의료인에게 정보통신기술을 활용하여 원격의료를 할 수 있도록 한 것을 DCT에 맞도록 임상시험용의약품을 원격지에 있는 임상시험대상자에게 처방을 가능하게 하는 개정안을 제안할 수도 있었지만, 이미 복지부 공고 제2020-177호 「전화상담·처방 한시적 허용방안」이 운영되었던 사례가 있어서 이를 같은 유형으로 보고 위와 같은 지침 마련을 제안했다.
셋째, 임상시험용의약품 택배 허용을 위한 위 「약사법」 제50조 제1항 개정안은, 의약품 배송이 「약사법」 제50조 제1항 위반이라는 판례, 즉, 대법원 2015. 9. 15. 선고 2014도13656 판결(https://glaw.scourt.go.kr)을 근거로 작성했다. 대법원은 의약품을 택배로 환자에게 배송하는 것은 약국개설자 및 의약품판매업자가 그 약국 또는 점포 이외의 장소에서 의약품을 판매한 것과 같다고 보았다. 따라서 임상시험용의약품 택배 허용을 위해서는 「약사법」 제50조 제1항을 개정해야 한다고 판단했으며, 예외 규정, 즉 “시장ㆍ군수ㆍ구청장의 승인을 받은 경우”에는 예외로 하는 조문에 ‘임상시험의 특성상 원격으로 데이터 수집이 가능하여 식품의약품안전처장이 승인한 임상시험의 임상시험용의약품의 배송’도 예외로 하는 것을 제안했다.
넷째, 먼저「의료법」제2조 제2항 제5호 마목을 신설할 것을 제안한 이유는 임상시험을 임상시험대상자의 거주지 또는 그와 유사한 장소에서 검체를 채취할 의료인으로 ‘가정간호사’가 적합하지 않고, 그 의미를 혼동할 수 있어 별도로 ‘임상시험 방문간호사’를 「의료법」제2조 제2항 제5호 마목에 신설하는 것을 제안함으로써 행위와 성격이 다른 ‘가정간호’와 ‘임상시험 방문간호’를 구분했다. 그리고, 「의료법 시행규칙」제24조의2를 신설하는 것을 제안한 이유는, 앞서 「의료법」제2조 제2항 제5호 마목에 ‘임상시험 방문간호사’를 신설했기 때문이며, 「의료법」 하위규정인 시행규칙에 상세한 ‘임상시험 방문간호사’의 역할과 조건을 명시하는 것이 타당하다고 보았다.4. 일관성 검증
일관성 지수(CR)가 0.2 이상일 경우 일관성이 부족한 것으로 판단하여, 수집된 설문 가운데 CR 값이 0.2 이상은 제외하고자 하였으나, 본 연구의 설문에서는 <표 4>와 같이 0.2를 넘는 설문은 없었으므로 일관성을 확보한 것으로 보았다. 다만, 평가자 B의 경우 0.2에 매우 근접하다 할 수 있어 평가자 B를 제외하는 것이 결과를 강력(robust)하게 하는 것일 수 있으나, 0.2가 기준인 만큼 평가자 B를 제외하지 않고 포함했다. 평가자의 이름은 영문 알파벳으로 비식별 처리하였다.
표 4. 일관성 분석구분 평가자A 평가자B 평가자C 평가자D 평가자E 평가자F 평가자G 평가자H 평가자I 평가자J 평가자K CR 0.116 0.198 0.186 0.186 0.000 0.105 0.136 0.070 0.070 0.040 0.000 Ⅲ. 연구결과
1. 중요도와 우선순위DCT를 제도적으로 도입하기 위한 상위요소(계층 1)의 상대적 중요도와 우선순위를 분석하면 <표 5>와 같다. DCT를 도입하기 위해 중점적으로 수행할 요소는 ‘임상시험실시기관 외 임상시험 허용’이 0.281, ‘임상시험용의약품의 택배 허용’이 0.193, ‘방문간호사의 검체 채취 허용’이 0.162, ‘임상시험용의약품의 원격처방 허용’이 0.111으로 나타났다. 즉, ‘임상시험실시기관 외 임상시험 허용’이 1순위, ‘임상시험용의약품의 택배 허용’이 2순위, ‘방문간호사의 검체 채취 허용’이 3순위, ‘임상시험용의약품 원격처방 허용’이 4순위로 나타났다.
표 5. DCT 도입을 위한 계층 1의 중요도 및 우선순위구분 중요도 우선순위 임상시험실시기관 외 임상시험 허용 0.281 1 임상시험용의약품의 택배 배송 허용 0.193 2 방문간호사의 검체채취 허용 0.162 3 임상시험용의약품 원격처방 허용 0.111 4
계층 1의 요소별, 평가자별 중요도는 <표 6>과 같다.
표 6. 계층 1 요소별 평가자별 중요도중요도 임상시험실시기관 외 임상시험 허용 임상시험용의약품 원격처방허용 임상시험용의약품의 택배 배송 허용 방문간호사의
검체채취 허용평가자 A 0.209 0.095 0.652 0.044 평가자 B 0.147 0.047 0.378 0.428 평가자 C 0.136 0.068 0.473 0.323 평가자 D 0.101 0.237 0.331 0.331 평가자 E 0.750 0.083 0.083 0.083 평가자 F 0.234 0.067 0.160 0.539 평가자 G 0.580 0.301 0.060 0.059 평가자 H 0.613 0.273 0.068 0.046 평가자 I 0.533 0.067 0.273 0.128 평가자 J 0.141 0.263 0.455 0.141 평가자 K 0.434 0.053 0.053 0.460 종합 0.281 0.111 0.193 0.162
2. 정책의 시행 vs 미시행상위요소(계층 1)의 중요도를 토대로 하위요소(계층 2)의 최종 중요도를 분석하였다. 본 연구에서는 DCT 제도 도입을 위한 4가지 요소를 기준으로 정책의 시행과 미시행의 중요도를 조사했다. 그 결과 <표 7>과 같이 4가지 요소에 대한 정책 시행 미시행을 종합한 결과는, 정책 시행이 0.657의 높은 평점을 얻었다. 정책 시행 대안이 정책 미시행 대안보다 상대적으로 높은 평점 0.5를 초과하는 점수를 얻으면 정책의 타당성이 있다는 결론을 도출하므로, 0.657을 얻은 정책 시행이 타당성이 있다고 할 수 있다.
표 7. 정책 시행 Vs 미시행구분 평점 정책 시행 0.657 정책 미시행 0.217
평가자별 정책 시행과 미시행에 대한 평가 결과는 <표 8>과 같다.
표 8. 평가자별 정책 시행 미시행 평가 결과평가자 정책 시행 정책 미시행 평가자 A 0.118 0.882 평가자 B 0.871 0.129 평가자 C 0.851 0.149 평가자 D 0.875 0.125 평가자 E 0.700 0.300 평가자 F 0.779 0.221 평가자 G 0.878 0.122 평가자 H 0.847 0.153 평가자 I 0.839 0.161 평가자 J 0.764 0.236 평가자 K 0.492 0.508 종합 0.657 0.217
<표 8>에는 11명의 평가자 중에서 9명의 평가자가 정책 시행에 더 높은 평점을 주었고, 반대 의견을 낸 평가자는 2명이었다. 반대 의견 2명 중에서 정책 미시행에 0.881의 더 높은 점수를 부여한 평가자 A를 설문조사 결과 분석 이후 별도로 인터뷰한 결과, 임상시험대상자의 검체나 임상시험용의약품이 배송될 때 온도 이탈 등 예상치 못한 문제가 발생할 가능성을 배제할 수 없기 때문에 DCT 제도 도입에 부정적 의견을 내었다고 밝혔다.Ⅳ. 논의
AHP 설문조사를 설계하면서 임상시험 산업의 진흥과 정책을 주도하는 국가임상시험지원재단과의 사전 인터뷰를 통해 계층1 요소3에 대해 법령 개정 사항이 아니라는 전문가의 주장이 있다는 사실을 확인했다. 즉, 임상시험용의약품은 허가받은 의약품이 아니므로 판매의 대상이 아니며, 의약품 택배 배송을 「약사법」 제50조 제1항을 위반하여 약국 외에서 의약품을 판매한 것으로 본 대법원 판례는 임상시험용의약품의 택배 배송에 적용하여 금지하는 것은 잘못된 법 해석이라는 주장이 그것이다.
의약품과 임상시험용의약품은 본질적으로 사람을 대상으로 약물을 적용한다는 점에서 공통점이 있으나, 몇 가지 중요한 차이점도 있다. 예컨대, 의약품은 이미 안전성과 유효성이 검증되어 환자 또는 소비자에게 제공되는 반면, 임상시험용의약품은 아직 연구 또는 시험의 과정에 있어 임상시험대상자만을 대상으로 사용된다는 점이 다르다. 또한, 의약품은 약국을 통해 최종 소비자 또는 환자에게 판매되지만, 임상시험용의약품은 임상시험실시기관이나 연구소를 통해 대상자에게 전달될 뿐 판매되지 않는다. 또한 이 과정은 매우 엄격하게 관리되고 있다. 따라서, 대법원의 판례는 의약품의 비약국 판매는 금지하고 있지만, 이 판례가 임상시험용의약품에도 동일하게 적용되는지를 판단하기 위해서는 좀 더 상세한 법적인 해석이 필요하다.
결론적으로, 임상시험용 의약품은 본질적으로 의약품이므로 기본적인 규제 원칙은 동일하게 적용될 수 있기 때문에, 본 연구에서 AHP 설문조사를 통해 전문가들에게 「약사법」 제50조 제1항 개정을 통한 ‘임상시험용의약품의 택배 배송 허용’을 다른 요소들과 함께 실험한 것에는 큰 오류는 찾을 수 없다. 다만, 임상시험용의약품이 대중에게 공개적으로 판매되는 것이 아니라 철저히 관리된 환경에서 직접 또는 택배로 전달되는 것을 법적으로 이를 '비약국 판매'로 간주할 것인지는 추가적인 전문가 델파이 조사 등을 통해 의견을 구체화할 필요가 있다.Ⅴ. 결론
전 세계는 기존의 임상시험 방식에서 DCT 방식을 빠르게 수용하여 의약품 개발을 촉진하고 있다. 이러한 글로벌 트렌드를 무시하고 기존의 방식만을 고집한다면 우리나라의 전 세계 임상시험 선도국의 위치는 한순간에 무너질 수도 있다. 다행히 정부는 이 규제지체현상의 심각성을 인지하고 DCT 허용을 위한 제도 검토와 시범사업을 추진 중이다. 하지만 「약사법」 등 관련 법령 정비가 필수적으로 수반되어야 하므로 이에 따른 시간이 불가피하게 소요된다.
본 연구는 DCT를 가능하게 하는 법령 정비를 보다 신속하게 할 수 있도록 선행연구 등을 통해 DCT 도입에 가장 우선되는 제도 개선과제가 무엇인지 조사하고, AHP 기법의 전문가 설문조사를 통해 해당 과제들의 우선순위와 중요도, 그리고 최종적으로 DCT 도입 정책 시행, 미시행 여부를 조사했다. 그 결과, DCT 도입 정책은 시행해야 하고, 이를 위해 가장 먼저 ‘임상시험실시기관 외 임상시험을 허용’에 대한 법제 개선이 가장 우선되어야 한다는 것으로 결론에 도달했다. 중요도 비교 결과, ‘임상시험용의약품의 택배 배송 허용’과 ‘방문간호사의 검체 채취 허용’, ‘임상시험용의약품의 원격처방 허용’은 ‘임상시험실시기관 외 임상시험 허용’보다는 상대적으로 중요도가 낮은 것으로 나타났다. 하지만, 중요도가 낮게 나왔다고 해서 이 과제들에 대한 법제 개선이 불필요하다는 의미는 아니며, 다만 정책담당자가 우선순위를 참고해서 최종 판단해야 할 것이다.
한편, 본 연구에서 확보한 전문가 집단의 수는 11명으로, AHP 기법 특유의 ‘전문성’ 차원에서는 어느 정도 표본을 확보한 것으로 볼 수 있다. 그러나, DCT 특성상 정보통신기술 분야 전문가의 의견을 청취하지 못한 부분은 본 연구가 가지는 한계점이라고 할 수 있다. 향후 연구에서는 더욱 정교한 중요도 도출 모형의 설정과 상세한 설명을 통해 DCT 특성에 맞는 통찰력을 제공할 수 있도록 해야 할 것이다.참고문헌
Clinical Trials Transformation Initiative. (2018). NEW CTTI RECOMMENDATIONS OFFER PATH FORWARD FOR DECENTRALIZED CLINICAL TRIALS. https://ctti-clinicaltrials.org/topics/mobile/new-ctti-recommendations-offer-path-forward-for-decentralized-clinical-trials/
EMA. (2022). Facilitating Decentralised Clinical Trials in the EU. https://www.ema.europa.eu/en/news/facilitating-decentralised-clinical-trials-eu
FDA. (2023). Decentralized Clinical Trials for Drugs, Biological Products, and Devices Guidance for Industry, Investigators, and Other Stakeholders https://www.fda.gov/regulatory-information/search-fda-guidance-documents/decentralized-clinical-trials-drugs-biological-products-and-devices
ITU. (2024). An overview of the state of digital develop the world based on ITU data. Digital Development Dashboard https://www.itu.int/en/ITU-D/Statistics/Dashboards/Pages/Digital-Development.aspx
IZEM, R. et al. Decentralized Clinical Trials: Scientific Considerations Through the Lens of the Estimand Framework. Therapeutic innovation & regulatory science, [s. l.], v. 58, n. 3, p. 495–504, 2024.
null. (2024). The landscape of decentralized clinical trials (DCTs): focusing on the FDA and EMA guidance. Translational and Clinical Pharmacology, 32(1), 41-51
김영호. (2022). 분산형 임상시험(Decentralized Clinical Trial): 장점과 사례 중심으로. Bio Economy Brief, Issue 147, 1-5.
대한민국 법원 종합법률정보. 대법원 2015. 9. 15. 선고 2014도13656 https://glaw.scourt.go.kr/wsjo/panre/sjo100.do?contId=2185824&q=%EC%9D%98%EC%95%BD%ED%92%88%20%ED%83%9D%EB%B0%B0%20%EB%B0%B0%EC%86%A1&nq=&w=panre§ion=panre_tot&subw=&subsection=&subId=2&csq=&groups=6,7,5,9&category=&outmax=1&msort=&onlycount=&sp=&d1=&d2=&d3=&d4=&d5=&pg=2&p1=&p2=&p3=&p4=&p5=&p6=&p7=&p8=&p9=&p10=&p11=&p12=&sysCd=WSJO&tabGbnCd=&saNo=&joNo=&lawNm=&hanjaYn=N&userSrchHistNo=&poption=&srch=&range=&daewbyn=N&smpryn=N&idgJyul=01&newsimyn=Y&trtyNm=&tabId=&save=Y&bubNm=
박득. (2015). AHP를 이용한 예비타당성평가. 한국컴퓨터정보학회논문지, 20(11), 163-168.
식품의약품안전처. (2023). 분산형 임상시험 도입 토대 마련을 위한 「임상시험 전자동의 가이드라인」 개정. https://www.mfds.go.kr/brd/m_99/view.do?seq=47936&srchFr=&srchTo=&srchWord=%EC%9E%84%EC%83%81%EC%8B%9C%ED%97%98&srchTp=0&itm_seq_1=0&itm_seq_2=0&multi_itm_seq=0&company_cd=&company_nm=&Data_stts_gubun=C9999&page=1
식품의약품안전처. (2024). ‘23년 의약품 임상시험 승인 ’22년 대비 10.1% 증가. https://www.mfds.go.kr/brd/m_99/view.do?seq=48253&srchFr=&srchTo=&srchWord=%EC%9E%84%EC%83%81%EC%8B%9C%ED%97%98&srchTp=0&itm_seq_1=0&itm_seq_2=0&multi_itm_seq=0&company_cd=&company_nm=&Data_stts_gubun=C9999&page=1
윤계형. (2020). 의약품 임상시험 안전 관련법제 개선 연구. 한국법제연구원, 연구보고 20-04.
이은영. (2020). 임상시험 관련 법제의 문제점과 개선방안. 동북아법연구, 13(3), 163-184.
이종한, 김신, 홍승헌, 김성부. (2020). 규제지체 해소를 위한 유연성 제고방안: 신산업중심으로. 한국행정연구원
허기영. (2023). "Factors influencing the reliability of decentralized elements in clinical trials: results of three prospective studies." 국내박사학위논문 서울대학교 대학원국문초록
연구목적: 2022년을 기점으로 글로벌 제약사들은 물리적 거리에 제약 없는 ‘분산형 임상시험(DCT)’을 적극 활용하고 있다. 환자 모집부터 검체 획득, 모니터링 등 임상시험 전 과정, 또는 상당 부분을 정보통신기술(ICT)을 활용해 원격으로 진행하는 임상시험을 DCT라 하는데, 다국가 임상시험에서 다양한 참가자 모집과 비용 절감, 환자 편의성 증대, 중앙 집중형 관리 등 장점으로 빠르게 확산되고 있다. 하지만 국내에선 「약사법」에 따라 지정된 임상시험실시기관 내에서만 임상시험이 허용돼 DCT는 현재 불법으로 인식되고 있다. 이런 상황에서 미국과 유럽, 중국 등 많은 국가들이 빠른 규제적 대처를 통해 글로벌 제약사 임상시험 수요를 빨아들이고 있다. 우리나라도 분산형 임상시험 허용을 위한 제도 검토와 시범사업을 추진 중이다. 하지만 「약사법」 등 관련 법령 정비가 필수로 수반되어야 하는 만큼 시간이 더 필요한 상황이다.
연구방법 본 연구는 정부가 신속하게 분산형 임상시험 제도를 도입할 수 있도록 「약사법」개정에 대한 규제 개선방안을 문헌검토를 통해 도출하고 AHP를 통해 전문가들로부터 의견을 구하고 그 중요도와 우선순위를 도출했다.
연구결과 그 결과, DCT 도입 정책은 시행해야 하고, 이를 위해 가장 먼저 ‘임상시험실시기관 외 임상시험을 허용’에 대한 법제 개선이 가장 우선되어야 한다는 것으로 결론에 도달했다.
주요어 : 분산형 임상시험, 약사법, 의료법, 규제개선, AHP국문 요약
전 세계는 기존의 임상시험 방식에서 DCT 방식을 빠르게 수용하여 의약품 개발을 촉진하고 있다. 이러한 글로벌 트렌드를 무시하고 기존의 방식만을 고집한다면 우리나라의 전 세계 임상시험 선도국의 위치는 한순간에 무너질 수도 있다. 본 연구는 DCT를 가능하게 하는 법령 정비를 보다 신속하게 할 수 있도록 선행연구 등을 통해 DCT 도입에 가장 우선되는 제도 개선과제가 무엇인지 조사하고, AHP 기법의 전문가 설문조사를 통해 해당 과제들의 우선순위와 중요도, 그리고 최종적으로 DCT 도입 정책 시행, 미시행 여부를 조사했다. 그 결과, DCT 도입 정책은 시행해야 하고, 이를 위해 가장 먼저 ‘임상시험실시기관 외 임상시험을 허용’에 대한 법제 개선이 가장 우선되어야 한다는 것으로 결론에 도달했다.
brokebutbusy 님의 블로그
정부지원 및 연구사업 공고 소식과 제안서 작성 꿀팁이었는데 접고 그냥 아무거나 씁니다.
