-
목차
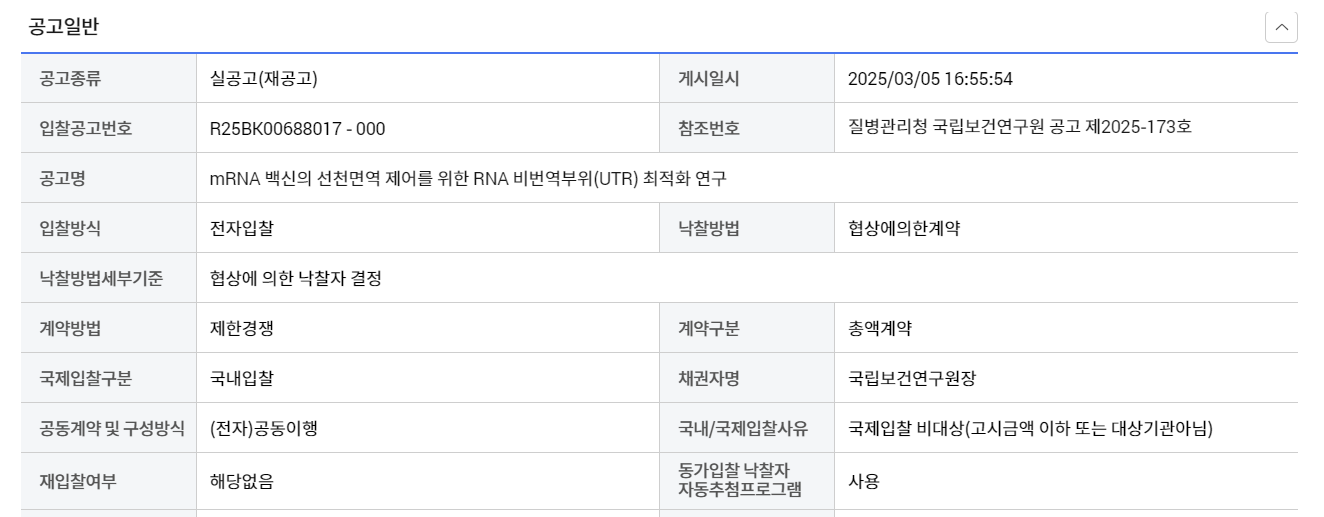
mRNA 백신의 선천면역 제어를 위한 RNA 비번역부위(UTR) 최적화 연구 1. 과제 개요
- 과제명: mRNA 백신의 선천면역 제어를 위한 RNA 비번역부위(UTR) 최적화 연구
- 발주기관: 질병관리청 국립보건연구원
- 연구비: 2억 원
- 연구기간: 계약일 ~ 2025.12.31.
- 계약방식: 제한경쟁
- 연구 목표: RNA 비번역부위(UTR)를 최적화하여 mRNA 백신의 면역반응 조절 및 백신 성능 개선
2. 연구 필요성
- mRNA 백신의 과잉 면역반응을 조절하고 항원 발현 효율을 증가시키는 기술 개발 필요
- 기존 mRNA 백신에서 슈도유리딘을 대체할 수 있는 RNA 요소 최적화 필요
- 국내 mRNA 백신 플랫폼 구축 및 치료제 개발을 위한 핵심 기술 확보 목표
3. 연구 내용
- In vitro 연구: RNA 비번역부위 길이, 개수, 위치 최적화 후 면역반응, 항원 발현, 안정성 평가
- In vivo 연구: 마우스 모델을 이용하여 백신 효과 검증 (선천면역, 적응면역 평가)
- 비교 연구: 최적화된 RNA 요소와 슈도유리딘 변형 핵산 백신 비교
- 데이터 분석: 실험 결과를 바탕으로 최적의 RNA 요소 조합 도출 및 특허 출원
4. 기대 성과
- 논문: SCI급 논문 1편 (상위 10% 내외)
- 특허: 국내·국외 특허 각 1건 출원
- 실용화: 국내 mRNA 백신 및 치료제 플랫폼 적용 → 글로벌 경쟁력 확보
- 사회적 효과: 감염병 예방 및 난치성 질환 치료제로 확장 가능
5. 입찰 관련 정보
- 참가 자격: 국가종합전자조달시스템(G2B) 등록 기업, 중소기업 및 소상공인 대상
- 선정 방식: 서면평가 또는 발표평가 후 협상에 의한 계약 체결
- 공동계약 가능, 하도급 불가
현재 mRNA 백신의 비번역부위(UTR) 최적화를 통한 선천면역 제어에 대한 국내외 연구는 활발히 진행되고 있습니다. mRNA 백신은 항원 단백질을 코딩하는 mRNA를 체내에 주입하여 면역 반응을 유도하는 방식으로, 이러한 mRNA의 5' UTR과 3' UTR은 mRNA의 안정성, 번역 효율성, 그리고 면역 반응에 큰 영향을 미칩니다.
특히, mRNA의 뉴클레오사이드 변형은 선천성 면역 반응을 조절하는 데 중요한 역할을 합니다. 이러한 변형을 통해 mRNA의 안정성과 번역 효율성을 향상시키고, 과도한 면역 반응을 억제하여 백신의 안전성과 효과를 높일 수 있습니다.또한, mRNA 백신의 전달체인 지질나노입자(LNP)의 조성 및 특성 조절을 통해 초기 면역 반응을 제어하고, T세포 반응을 활성화시키면서도 과도한 면역 반응을 낮추는 연구도 진행되고 있습니다.
이러한 연구들은 mRNA 백신의 효능과 안전성을 향상시키기 위한 다양한 전략을 모색하고 있으며, 향후 백신 개발에 중요한 기초 자료를 제공하고 있습니다.
mRNA 백신의 선천면역 제어를 위한 "RNA 비번역부위(UTR) 최적화"는 면역 반응을 조절하고 단백질 발현을 극대화하는 중요한 전략 중 하나입니다. 최적화 방법에는 여러 가지 접근법이 있는데, 주요 방법들을 정리해보았습니다.
1. 5' UTR 최적화
5' UTR(5' Untranslated Region)은 리보솜이 mRNA에 결합하는 과정과 초기 번역 효율에 영향을 미칩니다. 이를 최적화하면 단백질 발현을 증가시키면서 불필요한 선천면역 반응을 줄일 수 있습니다.
✅ 5' UTR 최적화 전략
- 코작 서열(Kozak sequence) 조정
- 강력한 Kozak 서열(예: GCCRCCaugG)을 도입하면 리보솜 결합을 향상시켜 번역 효율을 증가시킬 수 있습니다.
- 구아닌(G)-풍부 서열 회피
- 5' UTR에서 구아닌(G)이 많은 서열은 리보솜 결합을 방해할 수 있으므로 적절한 조정이 필요합니다.
- 스테미-루프(Stem-loop) 구조 조절
- 너무 강한 이차 구조는 번역을 저해할 수 있으므로 적절한 구조적 안정성이 필요합니다.
- 선천면역 회피를 위한 염기 변형 도입
- m1Ψ(1-methylpseudouridine)과 같은 변형 뉴클레오사이드를 포함하면 TLR(Toll-like receptor) 및 RIG-I 같은 선천면역 수용체의 활성화를 억제할 수 있습니다.
2. 3' UTR 최적화
3' UTR(3' Untranslated Region)은 mRNA의 안정성과 번역 효율을 결정하는 중요한 요소야. 최적화를 통해 mRNA의 반감기를 연장하고 면역 반응을 조절할 수 있습니다.
✅ 3' UTR 최적화 전략
- 안정적인 3' UTR 서열 도입
- 천연 mRNA에서 발견되는 안정성이 높은 서열(예: 알파 글로빈 mRNA의 3' UTR)을 활용하면 mRNA 안정성을 증가시킬 수 있습니다.
- AU-풍부 서열(AU-rich element, ARE) 제거
-
- AU-rich element는 mRNA 분해를 촉진하므로 제거하거나 최소화하면 반감기가 증가할 수 있습니다.
-
- Poly(A) tail 최적화
- Poly(A) tail 길이를 100~150nt로 조정하면 번역 효율과 mRNA 안정성을 높일 수 있습니다.
- 마이크로RNA(miRNA) 결합 사이트 회피
- 특정 miRNA가 mRNA 분해를 촉진할 수 있으므로, 면역 반응을 유도할 가능성이 있는 miRNA 타겟 서열을 제거하면 유익합니다.
3. 선천면역 회피를 위한 추가적인 RNA 최적화 기법
- 변형 뉴클레오타이드(m1Ψ, Ψ, 5mC) 도입
- m1Ψ(1-methylpseudouridine) 또는 Ψ(pseudouridine) 변형을 적용하면 RIG-I, MDA5, TLR3/7/8 같은 선천면역 센서를 회피할 수 있습니다.
- GC 함량 최적화
- 지나치게 높은 GC 함량은 mRNA의 이차 구조를 강화하여 번역 효율을 저하시킬 수 있으므로, 적절한 GC 비율(50~60%)을 유지하는 것이 중요합니다.
- 코돈 최적화
- 인간 세포에서 선호하는 코돈을 사용하면 단백질 발현을 증가시키면서 불필요한 면역 반응을 줄일 수 있습니다.
RNA UTR 최적화는 선천면역 반응을 조절하고, mRNA 백신의 안정성과 단백질 발현을 극대화하는 핵심 전략입니다.
- 5' UTR에서는 Kozak 서열 조정, 불필요한 이차 구조 회피, 변형 뉴클레오타이드 활용
- 3' UTR에서는 안정적인 서열 도입, Poly(A) tail 최적화, miRNA 타겟 회피
- 추가적으로 변형 뉴클레오타이드 사용과 GC 함량 조정으로 면역 반응을 조절 가능
'제안서' 카테고리의 다른 글
해양생물 고유특성 기반 바이오 신소재 개발 기획연구(1억2천만원) (0) 2025.03.17 췌장암 혁신 치료를 위한 AI 기반 방사성의약품 타겟 발굴 용역(5천만원) (0) 2025.03.10 항노화 및 역노화 첨단바이오의약품 기술개발 사업 기획연구(7천만원) (0) 2025.03.07 페길화 의약품 사용 현황 및 이상사례 실태조사(6천만원) (0) 2025.03.06 AI 기반 의료기기 안전관리 지원체계 구축 연구(9천만원) (0) 2025.03.06
brokebutbusy 님의 블로그
정부지원 및 연구사업 공고 소식과 제안서 작성 꿀팁이었는데 접고 그냥 아무거나 씁니다.
